Vacuna contra el Covid de Moderna muestra 100% de eficacia en infecciones graves
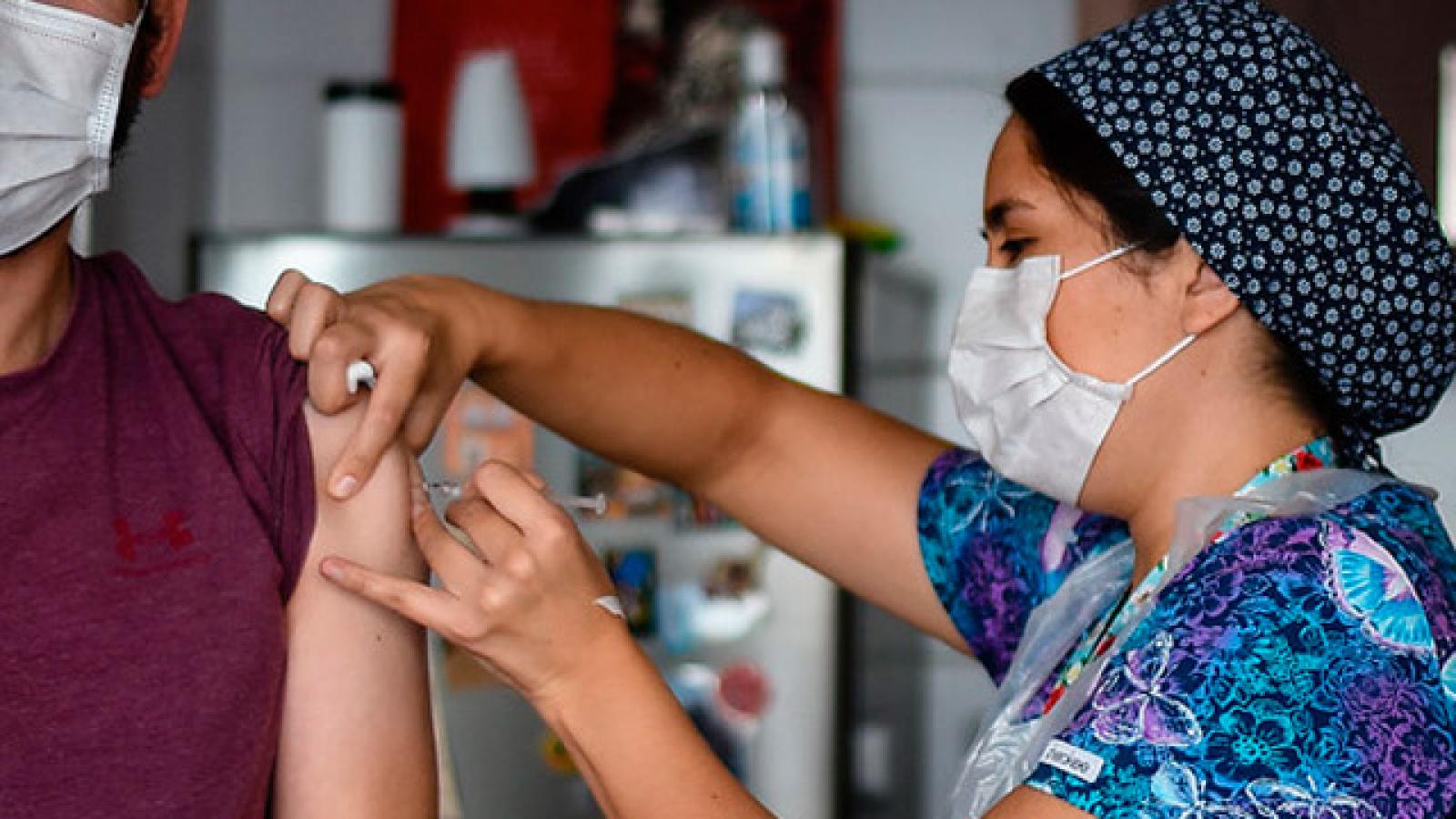
La compañía farmacéutica espera solicitar este lunes la autorización de su Vacuna contra el Covid ante la Administración de Drogas y Alimentos de EE.UU.
La empresa estadounidense de biotecnología Moderna, anunció que su Vacuna contra el COVID-19 tuvo una eficacia del 100% en infecciones graves.
De igual manera, la firma indicó que pretende solicitar este lunes la autorización para su antídoto ante la Administración de Drogas y Alimentos de EE.UU. (FDA).
La vacuna contra el coronavirus del laboratorio Moderna tendría un 94,1% de efectividad a la hora de prevenir el COVID-19 y sería un 100% efectiva en la prevención de casos graves de la enfermedad. Estos datos, deben corroborados por la FDA.
Moderna será la segunda empresa en solicitar a la Administración de Drogas y Alimentos de EE.UU. la autorización de uso de emergencia para la vacuna contra el COVID-19. La compañía farmacéutica Pfizer hizo lo propio el 20 de noviembre con datos que muestran una eficacia igualmente alta.
Revisa también: Bono Covid Navidad: Revisa aquí las comunas que recibirán el beneficio
La agencia reunirá en los próximos días para revisar ambas. El doctor Anthony Fauci, director del Instituto Nacional de Alergias y Enfermedades Infecciosas, señaló que si el proceso de revisión es exitoso, las primeras vacunas en Estados Unidos deberían tener lugar "hacia fines de diciembre".
¿Cómo funciona la autorización de emergencia para la vacuna contra el Covid?
La Administración de Drogas y Alimentos de EE.UU. Es la entidad gubernamental responsable de proteger la salud pública de dicho país y es la que garantiza la seguridad y eficacia de medicamentos, productos biológicos y dispositivos médicos de uso humano y veterinario.
La FDA (conocida por sus siglas en inglés) convoca a grupos de expertos estadounidenses e internacionales para que la ayuden a tomar sus determinaciones finales en base a la información que reciben, pues la información que posteriormente entregan, deben estar avalada en sólidos cimientos científicos.
Para este caso, el grupo de asesores se reunirá el 10 de diciembre para analizar los datos de la candidata de vacuna de Pfizer, proceso que puede durar uno o más días.


























